Lo importante para el ahorro de energéticos es que la realización de cada una de las tareas expuestas, es decir, la creación de un contraste y su exergía, demanda la destrucción de otros contrastes y, por lo tanto, de otras exergías existentes entre otros objetos. Se define la eficiencia de una tarea, también llamada eficiencia de la segunda ley de la termodinámica, denotada por la letra griega ε (epsilon), como:

Si los contrastes (exergías) que se crean son de la misma naturaleza que los contrastes (exergías) que se destruyen, siempre se ahorran energéticos.
Por ejemplo, la realización de la tarea mecánica de elevar un peso (creación de un Ch y una Exh), se puede efectuar de varias maneras: la mejor sería bajar otro peso (destrucción de otro Ch y otra Exh) empleando una palanca (véase figura 27), o poniendo a operar un motor eléctrico funcionando con energía eléctrica generada por medios también mecánicos: caídas de agua (destrucción de otro Ch y otra Exh ), aerogeneradores (destrucción de un Cp y una Exp).
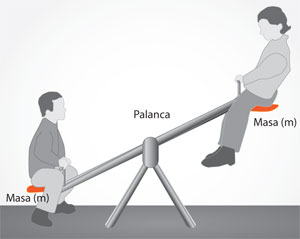
Cuando la exergía creada en la tarea es de la misma naturaleza que la exergía destruida, la eficiencia toma su valor máximo, que es 1.
Sin embargo, con frecuencia se emplean exergías de naturaleza diferente a la que exige la tarea; en el caso que se discute, empleando un motor eléctrico alimentado con la electricidad generada en una termoeléctrica. La exergía consumida para la generación de electricidad proviene del contraste químico del combustible con el ambiente. Si a ésta sumamos la exergía perdida en la transmisión de la corriente eléctrica y las pérdidas en la transformación a exergía gravitatoria, resulta que la Ex consumida total es mucho mayor que la Ex mínima requerida para efectuar la tarea. De este modo, resulta que ε < 1.
Otro ejemplo: la tarea de elevar la temperatura de una habitación de T0 a T2 (creación del contraste térmico CT = T2 – T0) se cumple incrementando, por ejemplo por calor Q2, la energía interna de la habitación hasta llegar a la temperatura confortable T2.
La cantidad mínima de trabajo (igual a la exergía mínima creada) que hay que invertir en esta tarea se puede calcular como sigue: el trabajo mínimo es igual, a su vez, al máximo trabajo que se puede obtener de Q2 , procesado de una caldera a la temperatura T2 frente al condensador a temperatura T0. Sabemos que este trabajo máximo es Q1/T2 CT, de modo que el numerador en la última ecuación es esta cantidad, entonces:
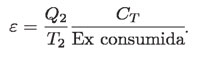
La cantidad Q2 de calor mínima necesaria para elevar la temperatura del cuarto se calcula, como antes se hizo, tomando en cuenta la capacidad térmica del aire (por ejemplo a presión constante) y el incremento de temperatura propuesto, así:
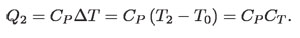
Q2 es la cantidad mínima de calor necesaria para calentar el cuarto en ΔT, porque el aire, a su vez, pasa energía a los demás objetos del cuarto. Por simplicidad, al no tomar este efecto en cuenta queda:
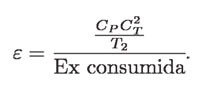
El valor final de ε depende de la exergía consumida, que es mucho menor empleando una bomba de calor que un calentador de resistencia, y aún menor si se consume la exergía de la radiación solar.