En general en la célula procarionte las moléculas no se encuentran en compartimientos delimitados por membranas, por lo que las funciones ocurren en el citoplasma. En las células eucariontes, las moléculas están distribuidas en compartimientos denominados organelos y en el citoplasma, y varios organelos tienen una estructura y función que permite la relación entre ellos. Se tratará ahora el tema los organelos relacionados con la expresión de muchos genes y, por ello, con el dogma central de la biología molecular, que se abordará en el tema de genética.
La mayoría de los genes eucariontes se encuentran en el núcleo, aunque también hay genes en las mitocondrias y en los cloroplastos. Todos los genes siguen un patrón de expresión genética explicado por el dogma central de la biología molecular. En esta sección trataremos principalmente de los genes localizados en el núcleo.
Los genes nucleares son el molde para la producción de ARN que se traducirá en proteínas, las cuales seguirán varias rutas en la célula o fuera de ella. Las proteínas que se sintetizan en los ribosomas se dirigen a los diferentes compartimientos gracias a la presencia de señales constituidas por secuencias específicas de aminoácidos. La mayoría de las proteínas que carecen de esta señal permanecerán en el citosol, mientras las que se destinan al núcleo, al retículo endoplásmico, al aparato de Golgi, a la mitocondria, al cloroplasto o a los peroxisomas, contienen señales particulares para la salida —como el péptido señal en el caso del retículo endoplásmico.
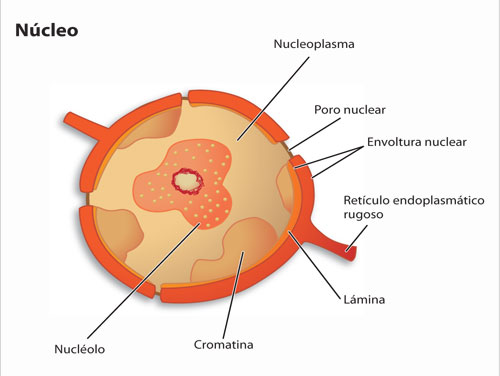
Núcleo | En los eucariontes la mayoría del genoma se localiza en el núcleo y a partir de ahí se expresan los genes. El ADN del genoma nuclear se asocia con proteínas específicas como las histonas y forman la cromatina, que puede ser compacta (heterocromatina) o extendida (eucromatina). La eucromatina es activa, pues el ADN puede ser copiado a ARN, mientras la heterocromatina es inactiva. El núcleo es un organelo delimitado por dos membranas que, en conjunto, se denomina envoltura nuclear. La membrana interna del núcleo se encuentra unida a una red de fibras de la lámina nuclear; mientras la membrana externa se conecta directamente con el retículo endoplásmico rugoso, de tal manera que el espacio entre las dos membranas se continúa con las cisternas del retículo. El intercambio selectivo de proteínas y moléculas de ARN entre el núcleo y el citoplasma se efectúa a través de los poros nucleares, los cuales, junto con moléculas de la matriz nuclear, desempeñan un papel importante en la regulación génica de los eucariontes.
Los núcleos en las células en crecimiento o metabólicamente activas replican ADN y sintetizan diferentes tipos de ARN: ribosomal, de transferencia, mensajero y los ARN pequeños nucleares, ricos en uracilo (llamados en inglés small nuclear sRNA o snRNAs), en diferentes lugares o dominios del núcleo: los ARN mensajeros se producen en el nucleoplasma, el ARN ribosomal en el nucléolo.
Ribosomas y retículo endoplásmico rugoso | Las proteínas se forman por la unión de aminoácidos a través del enlace peptídico, que en la célula ocurre en el ribosoma. El ribosoma es una estructura pequeña, de aproximadamente 15 μm de diámetro, formada por proteínas y el ARNr, agrupados en dos subunidades, una pequeña y una grande —hoy en día se conoce la posición de cada una de las moléculas que forman a los ribosomas. Pueden estar libres en el citoplasma o unidos a membranas del retículo endoplásmico rugoso.
Las proteínas que se forman en el ribosoma a partir de ARNm pueden seguir al menos dos rutas: 1] forman parte del citoplasma y 2] siguen la ruta secretora. En el primer caso, las proteínas se sintetizan en ribosomas libres y en el segundo, los ribosomas se asocian con el sistema de membranas del retículo endoplásmico rugoso.


El retículo endoplásmico es una red de sacos aplanados o cisternas, túbulos y vesículas que se encuentra constituida por una membrana continua que limita un espacio denominado lumen. Este organelo se encuentra diferenciado en una región cubierta con ribosomas llamado retículo endoplásmico rugoso (RER) y otra zona tubular que carece de ellos, denominada retículo endoplásmico liso (REL).
El papel del RER fue reconocido por George Palade alrededor de 1960, al estudiar el destino de las enzimas digestivas secretadas por las células pancreáticas. Palade y sus colaboradores siguieron el rastro de las proteínas recién sintetizadas y las encontraron en el RER, en el aparato de Golgi y finalmente en las vesículas de secreción que, al fusionarse con la membrana plasmática, liberaban su contenido al exterior. Finalmente se reconoció que no sólo las proteínas de secreción pasaban por el retículo endoplásmico, sino también las que se incorporaban al mismo retículo, al aparato de Golgi y las destinadas a los lisosomas y a la membrana celular.
Los ribosomas libres que sintetizan el resto de las proteínas codificadas por el genoma nuclear son iguales a los asociados con las membranas del RER, y la diferencia estriba en que cuando un ribosoma está sintetizando una proteína que porta una secuencia señal, ésta compromete al ribosoma para asociarse con el RER. El reconocimiento de la secuencia señal se debe a los trabajos de Günther Blobel y David Sabatini, quienes en 1971 propusieron la existencia de una secuencia de aminoácidos que determinaba la localización de un producto proteico. Blobel recibió el Premio Nobel por este descubrimiento.
El RER es el lugar en donde se efectúa el plegamiento de las proteínas, el ensamblaje de las proteínas con estructura cuaternaria y donde se inicia la adición de carbohidratos (glicosilación). Además, el RER es un sitio de control que elimina las proteínas que no se han plegado correctamente; por ejemplo, una proteína mal plegada es exportada del organelo, antes de que llegue al complejo de Golgi, para que sea destruida por los proteasomas.
Las proteínas destinadas a la membrana plasmática o a las membranas del retículo endoplásmico, del complejo de Golgi o a la de los lisosomas, se insertan en la membrana del retículo en lugar de liberarse en su lumen. De esta manera se transportan hasta llegar a su membrana de destino.
Retículo endoplásmico liso (REL) | Las regiones del retículo que carecen de ribosomas y que presentan una estructura tubular reciben el nombre de retículo endoplásmico liso (REL). Es muy abundante en células que sintetizan gran cantidad de lípidos, por ejemplo, las que sintetizan hormonas esteroides, a partir de colesterol.
Puesto que los lípidos son muy hidrofóbicos, su síntesis no puede llevarse a cabo en el citosol. Los lípidos recién sintetizados en el REL son transportados por medio de vesículas o mediante proteínas acarreadoras, como ocurre en los hepatocitos, en los cuales el colesterol es transportado por medio de micelas lipoproteicas.
La membrana del REL sintetiza casi todos los lípidos necesarios para la formación de membranas. La síntesis de estos lípidos ocurre en la capa de fosfolípidos que está en contacto con el citosol, donde se encuentran todas las sustancias necesarias para la síntesis, por ejemplo, ácidos grasos y glicerol. Posteriormente, los lípidos recién formados son transferidos a la capa que está en contacto con el lumen del retículo, equilibrándose de este modo la cantidad de lípidos que deben encontrarse en la membrana.
El REL está también involucrado en la destoxificación de drogas, en el metabolismo de los carbohidratos y en el almacenamiento del calcio. En el primer caso, el retículo usa una serie de enzimas que convierten a las drogas hidrofóbicas en moléculas solubles en agua, para que sea fácil expulsarlas de las células por medio de la orina.
El REL de los hepatocitos también juega un papel importante en el metabolismo de los carbohidratos. Por la acción de una enzima que se encuentra unida a la membrana del REL, la glucosa almacenada en el hígado en forma de glucógeno, puede salir hacia la sangre para ser transportada a las células que necesiten de energía.
En ciertas células, como las musculares, el REL sirve también como sitio de almacenamiento de calcio, que es liberado en respuesta a determinadas señales, desencadenando la contracción muscular.
Aparato de Golgi | Las proteínas provenientes del retículo endoplásmico llegan al aparato de Golgi, donde terminan su procesamiento; de ahí se distribuyen por tres posibles vías: a los lisosomas, a la membrana o al exterior de la célula. Además, algunos lípidos, como la esfingomielina, son sintetizados en este organelo, al igual que los polisacáridos que forman la pared celular de las células vegetales.
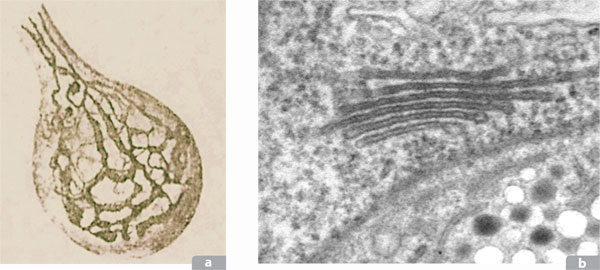
Esta estructura recibe su nombre por Camilo Golgi, biólogo italiano, quien en 1898 reportó una estructura presente en las células nerviosas que se ponía de manifiesto con tetraóxido de osmio. No obstante, la presencia del aparato de Golgi no se aceptó hasta la década de 1950, cuando se confirmó su existencia al ser observado con el microscopio electrónico.
Este organelo consiste en un conjunto de sacos aplanados, ensanchados en las orillas, paralelos entre sí, cuyo número varía según la actividad metabólica que realice la célula. Los sacos se encuentran rodeados de numerosas vesículas de transporte que se desprenden o que llegan a él. Las proteínas, procedentes del RER, ingresan en el organelo por su cara convexa denominada cis, que se encuentra normalmente orientada hacia el núcleo, y pasan de un saco a otro, hasta salir finalmente por la cara trans, después de haber sido modificadas.
La función primordial del aparato de Golgi es continuar con el proceso de glicosilación iniciado en el retículo endoplásmico. Es decir, termina la formación de glicoproteínas, incluida la modificación y síntesis de nuevos azúcares para, finalmente, constituir una enorme variedad de oligosacáridos, que darán especificidad a las proteínas que los posean. Asimismo, es en el aparato de Golgi donde se forman las proteínas ricas en azúcares características de la matriz extracelular y del mucus que recubre muchos epitelios.
Los lípidos y las proteínas finalmente son exportados hacia su lugar de destino por medio de vesículas que se desprenden de la región trans del aparato de Golgi; esto es posible porque las proteínas poseen una "etiqueta" (por ejemplo, una determinada secuencia de aminoácidos o un oligosacárido específico) que les permite llegar a su sitio de destino y permanecer en él.
Si bien, el RER y el aparato de Golgi son distintos desde el punto de vista de su actividad metabólica, en realidad se presenta una continuidad física debida a la presencia de las vesículas de transporte que mantienen un flujo constante entre ellos y los otros organelos membranosos; las mitocondrias y los cloroplastos son los únicos que no participan en la comunicación permanente a través de vesículas.

Lisosomas | Estos organelos están delimitados por una membrana y provienen del aparato de Golgi, contienen cerca de 50 tipos diferentes de enzimas hidrolíticas; participan en la digestión intracelular de sustancias tomadas del exterior, así como en la eliminación de organelos que la célula debe desechar. Presentan gran variedad en cuanto a forma y tamaño se refiere, dependiendo del material que se va a digerir.
Son característicos de las células animales, aunque las plantas y los hongos poseen vacuolas, que por su contenido de enzimas hidrolíticas, se relacionan con los lisosomas; sin embargo, las vacuolas efectúan además otras funciones.
Los lisosomas fueron descubiertos a principio de la década de 1950, por Christian de Duve y sus colegas. El análisis químico de estos organelos, aislados por medio de centrifugación, mostró que contenían diversas enzimas hidrolíticas, entre las que se encontraban proteasas, fosfatasas, ribonucleasas y desoxirribonucleasas. Debido a que el organelo tenía a su cargo la función de la lisis celular, de Duve les dio el nombre de lisosomas.
Una de las funciones mejor estudiadas de los lisosomas es la degradación de las sustancias que entran en la célula por endocitosis. Las sustancias ingresan mediante invaginaciones de la membrana, las cuales se transforman en vesículas que posteriormente se fusionan con endosomas primarios. Algunas de las moléculas ingeridas pueden regresar a la membrana, mientras los endosomas primarios se transforman en endosomas secundarios cuando adquieren las enzimas digestivas de vesículas procedentes del aparato de Golgi. Los endosomas se convierten en lisosomas maduros cuando inician su actividad digestiva. El interior de estos organelos tiene un pH ácido, que es el ideal para que sus enzimas funcionen óptimamente.
La digestión se lleva a cabo en el interior de los lisosomas; pero, en ocasiones, se libera su contenido hacia el exterior por exocitosis, por lo que ocurre una digestión extracelular. En la fecundación, por ejemplo, el espermatozoide descarga las enzimas que se encuentran en el acrosoma, que es un derivado del aparato de Golgi y cuya función es la de digerir las cubiertas del óvulo para que pueda penetrar el espermatozoide. En el caso de enfermedades como la artritis reumatoide, es posible que los problemas que se presentan sean debidos a la liberación del contenido lisosomal en las articulaciones. Se han identificado hasta la fecha cerca de 40 enfermedades relacionadas con el almacenamiento anormal de sustancias en los lisosomas. Estos padecimientos se deben a mutaciones en los genes que codifican la síntesis de las enzimas del lisosoma y que, en general, están relacionadas con la degradación de lípidos o de polisacáridos o con el transporte de los productos de digestión fuera del lisosoma. Las sustancias no degradadas o no transportadas fuera del organelo se acumulan, provocando graves daños en el organismo, como los producidos por las enfermedades de Tay-Sachs o de Gaucher, que además de causar desórdenes mentales, ocasionan un aumento de tamaño en el hígado y el bazo, además de lesiones en hueso.
El proceso de exo-endocitosis está relacionado también con el movimiento de sustancias que (además de hacerse mediante proteínas acarreadoras, canales proteicos o bien por simple difusión) se produce a menudo por invaginación o fusión de las membranas. La entrada de moléculas, micelas e incluso células, se hace mediante endocitosis, que consiste en una invaginación de la membrana, la cual pronto se desprende para formar una vesícula endocítica.
El nombre de endocitosis fue acuñado por de Duve en 1963, e incluye la ingestión de células o partículas grandes (fagocitosis) y la ingestión de fluidos o macromoléculas (pinocitosis). En todas las células eucariontes se realiza la pinocitosis, pero sólo algunas células especializadas efectúan la fagocitosis (por ejemplo, macrófagos y neutrófilos de los mamíferos y algunos protozoarios).
Durante la fagocitosis, la adhesión de la partícula a la membrana del fagocito, desencadena la actividad del citoesqueleto para que se formen los seudópodos, que rodean el cuerpo ingerido hasta formar grandes vesículas denominadas fagosomas; éstos se fusionan con los endosomas o se convierten en lisosomas en los que se digiere el material englobado. En la pinocitosis, las células continuamente forman pequeñas invaginaciones de membrana que indiscriminadamente toman del medio, líquido y moléculas disueltas en él; pero existe otro tipo de endocitosis que requiere de un receptor específico para una molécula determinada.
Michel Brown y Joseph Goldstein obtuvieron el Premio Nobel en 1986 por el descubrimiento de la endocitosis mediada por receptor, cuando estudiaban la hipercolesterolemia familiar, enfermedad hereditaria que se caracteriza porque el gen que codifica para el receptor de una partícula que lleva el colesterol a las células de los mamíferos —micela de LDL (lipoproteína de baja densidad)— se encuentra mutado y, como consecuencia, la micela no puede ingresar en la célula, lo que provoca la elevación de los niveles de colesterol sanguíneos, únicamente en animales.
El análisis de cómo se forman los receptores para las micelas de LDL, de cómo se interna la micela en la célula y de cuál es su destino, constituye un interesante ejemplo de la interrelación entre los diferentes organelos y las moléculas que participan en el proceso. Éste se inicia con la unión de la micela de LDL con el receptor que se encuentra en una invaginación de la membrana. Inmediatamente después, la invaginación se cierra formando una vesícula endocítica, rodeada por diversas proteínas. Éstas se desprenden de la vesícula, la cual se fusiona con un endosoma secundario. El pH ácido de este organelo provoca una modificación en la conformación del receptor y de la proteína de la micela, lo que los obliga a separarse. El receptor es transportado hacia la membrana plasmática por medio de una vesícula para reciclarse.
El endosoma secundario que lleva la partícula de LDL se fusiona con las vesículas procedentes del aparato de Golgi que contienen las hidrolasas. La partícula es digerida y sus aminoácidos son transportados hacia el citoplasma para reutilizarse en la síntesis de nuevas proteínas. El colesterol se incluirá en la membrana plasmática o, dependiendo de la célula, se usará como base para hacer hormonas esteroides o sales biliares.
Por otro lado, la síntesis de los receptores de las partículas de LDL es dirigida por su gen correspondiente, y su transcripción se regula de acuerdo con la cantidad de colesterol que exista en la célula y la necesidad que se tenga de esa sustancia. El ARNm producto de la transcripción del gen sale del núcleo hacia el citosol, donde se inicia la síntesis del receptor. Como el receptor está destinado a la membrana celular, la síntesis del mismo se continúa en el interior del RER, donde se pliega y se inicia su glicosilación. La proteína, a continuación, pasa al aparato de Golgi para terminar su proceso de formación. Finalmente, una vesícula que se desprende del aparato de Golgi llevará el receptor hacia la membrana plasmática.
Peroxisomas | Se trata de organelos rodeados de una sola membrana, que contienen enzimas involucradas en diversos procesos metabólicos. Desde el punto de vista morfológico son similares a los lisosomas, y derivan del retículo endoplásmico. Se encuentran en todas las células eucariontes, pero son muy abundantes en las células del hígado y de los riñones de los mamíferos, así como en las algas y en las células fotosintetizadoras de las plantas, y en las semillas oleaginosas en germinación.
El peroxisoma, al igual que las mitocondrias, utiliza la mayor parte del oxígeno disponible en las células. Por esta razón, este organelo tuvo como función original la de bajar el nivel del oxígeno presente en las células primitivas, protegiéndolas de la acción tóxica de este gas. En el transcurso de la evolución, las mitocondrias empezarían a utilizar con ventaja el oxígeno, acoplándolo a la producción de energía por medio de la fosforilación oxidativa.
Al igual que en los lisosomas, existen enzimas que están involucradas en diversas vías metabólicas que varían según el tipo de célula de que se trate. Cuando los peroxisomas fueron descubiertos se encontró la catalasa, una enzima que descompone el peróxido de hidrógeno, lo que le dio el nombre a estos organelos.
Los peroxisomas también se relacionan con el metabolismo de los lípidos, tanto en lo que respecta a su síntesis, como a su degradación. Por ejemplo, participan en las primeras reacciones de síntesis de los plasmalógenos, que son fosfolípidos especiales muy abundantes en las vainas de mielina del tejido nervioso.
Debido a la gran cantidad de funciones que realizan, no es de sorprender que existan las llamadas enfermedades peroxisomales, producidas por mutaciones que afectan la síntesis de las proteínas de estos organelos. La enfermedad más común es la adrenoleucodistrofia, en la que una proteína de membrana defectuosa impide el paso de los ácidos grasos de cadena larga al interior del peroxisoma, para que se efectúe su destrucción; la acumulación de los ácidos grasos en los fluidos del cuerpo ocasiona la degeneración de la vaina de mielina del tejido nervioso.
En las plantas y en las algas, los peroxisomas también desempeñan importantes funciones. En las semillas oleaginosas son los responsables de transformar los ácidos grasos almacenados en carbohidratos necesarios para proporcionar energía y materiales de construcción para la planta en germinación. La vía metabólica que permite estos cambios se denomina ciclo del glioxilato, una variante del ciclo de Krebs; por esta causa los peroxisomas que desempeñan esta función se denominan glioxisomas.
En las células de las hojas, los peroxisomas, en estrecha colaboración con las mitocondrias y los cloroplastos, realizan la fotorrespiración, que aparentemente es un proceso no esencial para la vida. La enzima que en la fotosíntesis permite la fijación del CO2 para iniciar la síntesis de la glucosa, en la fotorrespiración fija oxígeno y desprende CO2, sin la producción de ATP. Esto constituye una pérdida para la planta, pues casi un tercio del CO2 se pierde en este proceso. La enzima fija oxígeno o bióxido de carbono dependiendo de la concentración de estos gases; si el
CO2 es abundante, la enzima lo fija y se realiza el ciclo de Calvin; si, por el contrario, el oxígeno es más abundante, se llevará a cabo la fotorrespiración.
En el interior de las células eucariontes se presentan organelos cuyo papel principal es el de generar moléculas energéticas por la oxidación de los nutrientes. Éste es el caso de mitocondrias y cloroplastos, cuya estructura y función se verá en esta sección.
La clave para el mantenimiento de la vida radica en la capacidad de los organismos para utilizar la energía que proporcionan las reacciones termonucleares del Sol y la que se encuentra en los compuestos químicos. La molécula energética común en todos los sistemas vivos es el ATP (adenosín trifosfato) que conserva su energía en los enlaces de fosfato que se emplean en todo tipo de trabajo celular.
Mitocondrias | Son pequeños organelos de formas variadas, sumamente plásticos, que miden alrededor de 0.5 μm de ancho y casi 7 μm de largo. Se encuentran en casi todas las células eucariontes. Su número varía, desde una o muy pocas en muchos protozoarios, hongos y algas, también se localizan en mayor abundancia en ciertas regiones de la célula que requieren de mayor cantidad de ATP. hasta varios cientos o incluso miles en algunas células de plantas y animales. La cantidad de mitocondrias en una célula varía no sólo de acuerdo con la actividad metabólica de la misma; también se localizan en mayor abundancia en ciertas regiones de la célula que requieren de mayor cantidad de ATP.



Se tuvo noticia de estos organelos desde 1850, cuando Rudolph Kölliker los descubrió en las células musculares; al notar que estas partículas se hinchaban cuando se colocaban en agua, dedujo que estaban rodeadas por una membrana semipermeable.
Su papel en el metabolismo oxidativo empezó a estudiarse desde principios del siglo XX por investigadores como Otto Warburg, quien demostró que estos gránulos aislados consumían oxígeno. Pero fue hasta el descubrimiento de la técnica de centrifugación diferencial cuando estos organelos pudieron ser estudiados más a fondo por científicos destacados como Hans Krebs, Eugene Kennedy y Albert Lehninger, quienes dieron a conocer las reacciones del ciclo del ácido cítrico y el transporte de electrones y la fosforilación oxidativa, que constituyen la respiración celular.
Las mitocondrias son organelos rodeados de dos membranas, una externa y una interna plegada que aumenta su superficie total. La zona limitada por la membrana interna recibe el nombre de matriz y la zona que se encuentra entre las dos membranas se denomina espacio intermembranal, ambas de naturaleza acuosa.
La membrana externa es bastante permeable a iones y pequeñas moléculas, gracias a la presencia de proteínas transmembranales llamadas porinas. La membrana interna sólo permite el paso de piruvato, ácidos grasos, ATP, ADP y fosfato inorgánico, entre otros. Igualmente, presenta complejos proteicos involucrados en el transporte de electrones, en la translocación de protones y en la síntesis de ATP.
Las crestas formadas por el plegamiento de la membrana interna reflejan la actividad de una determinada célula; las células con gran actividad metabólica, como las células musculares de los colibríes, tienen gran cantidad de crestas; en cambio, las células de los vegetales, que tienen bajas tasas respiratorias, poseen mitocondrias con pocas crestas.
En la matriz acuosa se encuentra la mayoría de las enzimas involucradas en la función de este organelo; hay también aquí ADN circular, ARN y los ribosomas, que le dan a la mitocondria una independencia genética casi completa.
La mitocondria es el centro metabólico por excelencia donde, mediante la oxidación de moléculas combustibles, se sintetiza la mayor parte del ATP que requieren las células eucariontes.
Su similitud con las bacterias llevó a la propuesta de que las mitocondrias habían sido bacterias de vida libre adoptadas por alguna célula hospedera para vivir como endosimbiontes. Lynn Margulis recuperó esta hipótesis y acumuló evidencias que no dejan lugar a dudas respecto al origen bacteriano de estos organelos, como la presencia de ADN circular (semejante al ADN bacteriano) y sensibilidad a los mismos antibióticos.
De acuerdo con Margulis, en el arqueano, la proliferación de las cianobacterias fotosintetizadoras propició el aumento de oxígeno en la atmósfera. Muchas de las bacterias incapaces de soportar el oxígeno murieron o se refugiaron en zonas a las cuales no llegaba este gas, mientras otras desarrollaron un sistema de protección frente a la extrema toxicidad del oxígeno. Estas bacterias aerobias, que poseían ya un sistema enzimático parecido al de las mitocondrias actuales, establecieron una relación estable con otros eucariontes primitivos de mayor tamaño, que se habían convertido en fagocitadores.
Primeramente se establecería una relación de depredador-presa, en la cual las células aerobias serían engullidas como alimento. Con el tiempo, algunas de estas presas desarrollarían una cierta tolerancia para permanecer largos periodos dentro del citoplasma del huésped. Posteriormente, y debido a que los aerobios instalados en su citoplasma usaban el oxígeno que se encontraba en ciertos ambientes, los anaerobios hospederos pudieron gradualmente adentrarse en ambientes ricos en oxígeno sin ningún peligro.
Gradualmente, hospederos y huéspedes se hicieron mutuamente dependientes, marcando uno de los hitos más importantes en la evolución de la célula eucarionte.
En la actualidad, las mitocondrias utilizan con gran eficacia el oxígeno y se han convertido en potentes generadores de ATP, es decir, efectúan la combustión de los metabolitos procedentes de los nutrientes (carbohidratos, lípidos y proteínas) para sintetizar la molécula energética por excelencia, de la cual depende en gran medida la vida.
El genoma mitocondrial humano está constituido por 16 569 pares de bases y contiene únicamente 37 genes. Trece de éstos codifican para proteínas relacionadas con la producción de energía, es decir, proteínas pertenecientes a la cadena respiratoria; las restantes 24 codifican para moléculas de ARN que corresponden a ARN de transferencia para cada aminoácido, así como genes para los ARN ribosomales de la mitocondria: 12S y 16S. Las demás funciones mitocondriales son codificadas por genes nucleares; una vez que las proteínas son sintetizadas en el citoplasma se exportan al interior de la mitocondria.
Los genes del genoma mitocondrial están muy cercanos entre sí y no contienen intrones, hecho que hace que este genoma sea más parecido a los genomas bacterianos, lo que constituye una evidencia del origen procarionte de estos organelos.
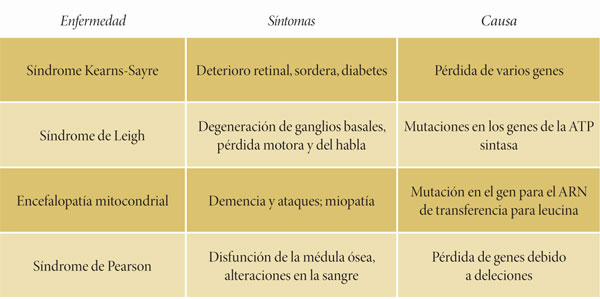
Las mutaciones ocurridas en el genoma mitocondrial provocan una alteración en el metabolismo energético que causa diversas enfermedades que pueden afectar al sistema nervioso central, la vista, el oído, el corazón, el músculo esquelético, los riñones y el sistema endocrino.
Las enfermedades mitocondriales no siguen el patrón mendeliano debido principalmente a que las mitocondrias sólo se heredan por vía materna, por lo que este tipo de enfermedades lo harán de la misma manera. La mayoría de las enfermedades debidas a mutaciones en el genoma mitocondrial tienden a manifestarse en el transcurso de la vida del individuo y se agravan conforme avanza la edad, pues el efecto de la mutación aumenta con el tiempo, al incrementarse la cantidad de genomas afectados.

Cloroplastos | Una vez que las mitocondrias se adaptaron a su vida en el primitivo fagocito, otro episodio de endosimbiosis se presentó en algunas de estas nuevas células. Un endosimbionte diferente habría de cambiar las estrategias para la obtención de alimento. Las células que obtuvieron la ventaja de poseerlos prosperaron rápidamente, pues sólo necesitaban para sintetizar su alimento aire, agua, energía solar y sales minerales en disolución que su medio les proporcionaba en abundancia. Con el tiempo, estos nuevos endosimbiontes se convirtieron en plástidos, que son los organelos característicos de las algas pardas, rojas y verdes y de las plantas que posteriormente evolucionaron a partir de éstas. Hay diversos tipos de plástidos, pero sólo los cloroplastos efectúan la fotosíntesis.
Existe una gran similitud entre las mitocondrias y los cloroplastos, pues ambos organelos generan ATP, contienen su propio genoma (no asociado a histonas) y se dividen por partición. Pero, además de fijar el CO2, los cloroplastos sintetizan aminoácidos y ácidos grasos y realizan la reducción de nitrito (NO2) a amonio (NH3) indispensable para que el nitrógeno se incorpore a los compuestos orgánicos.
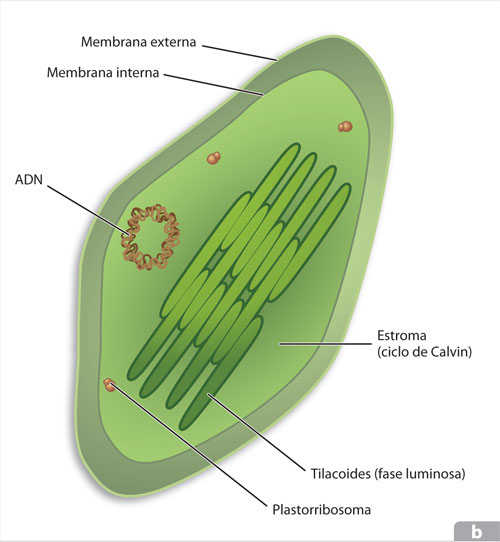
Los cloroplastos son organelos muy grandes, de 5 a 10 μm de longitud. Al igual que las mitocondrias, se encuentran rodeados por una doble membrana. Adicionalmente, poseen un sistema de membranas internas denominadas tilacoides, que en determinados sitios se pliegan sobre sí mismas formando sacos tilacoidales que agrupados constituyen los grana. La compartimentación de los cloroplastos es más complicada que en la mitocondria. En los cloroplastos se encuentra: 1] un espacio entre las membranas de la envoltura; 2] el estroma que es la zona que se encuentra entre la envoltura y las membranas tilacoidales, y 3] el lumen tilacoidal.
A pesar de la complejidad que muestran estos organelos, puede establecerse una similitud interesante con la mitocondria. En la membrana externa de ambos organelos se localizan porinas que facilitan la entrada a iones y pequeñas moléculas. Sin embargo, la membrana interna impide el paso de iones y metabolitos que sólo pueden acceder al interior del cloroplasto mediante transportadores específicos. Por su parte, el estroma del cloroplasto es equivalente a la matriz de la mitocondria, pues contiene el material genético y un conjunto de enzimas entre las cuales se encuentran las que intervendrán en la síntesis de los carbohidratos.
La diferencia más notable entre ambos organelos radica en las funciones que realizan sus membranas. En la mitocondria, la membrana interna plegada en crestas es la responsable del transporte de electrones, de la translocación de protones y de la quimiosmosis, que lleva a la síntesis de ATP; en cambio, la membrana interna del cloroplasto no participa en la fotosíntesis; este papel se ha reservado a las membranas tilacoidales. Es en estas membranas donde se localizan los fotosistemas, las sustancias destinadas al transporte de los electrones y a la traslocación de protones y la ATP sintasa.
Los cloroplastos tienen una gran similitud con las células procariontes; por ejemplo, el tamaño y la forma, así como la presencia de ADN circular o ADN cloroplástico; también llevan a cabo en su interior síntesis de proteínas y se dividen de una manera semejante a las bacterias.
De acuerdo con lo anterior, no es de extrañar que también existan similitudes en cuanto a las características de los procesos energéticos que se dan en estos organelos y las bacterias. Por ejemplo, tanto la respiración celular como la fotosíntesis ocurren en dos fases: una soluble y otra no soluble, de manera similar a lo que sucede en las bacterias.
Mientras la fase soluble de la respiración y de la fotosíntesis se lleva a cabo en la matriz mitocondrial y en el estroma del cloroplasto, en las bacterias esto ocurre en el citoplasma. Asimismo, la fase no soluble se asocia con la membrana interna mitocondrial y con las membranas tilacoidales, de una manera semejante a lo que ocurre con la membrana celular de las bacterias aerobias y de las fotosintéticas.
Así, la fotosíntesis consiste de dos fases: una luminosa —síntesis de ATP y NADPH— y otra oscura —síntesis de azúcares.
Otros plástidos | Además de los cloroplastos (que en las angiospermas y en las gimnospermas se encuentran en las hojas, los tallos jóvenes y los frutos no maduros), en las plantas se localiza una variedad de plástidos que realizan diversas funciones. Éstos, a diferencia de los cloroplastos, carecen de tilacoides y de los integrantes del sistema fotosintetizador. Se clasifican según el tipo de pigmentos que poseen: 1] cromoplastos que contienen carotenoides, responsables de los colores amarillo y anaranjado de frutas y flores, su papel en el metabolismo no es claro; 2] leucoplastos incoloros que actúan como reservorios de materiales energéticos; 3] amiloplastos y elaioplastos, variedades de leucoplastos que acumulan almidón y lípidos, respectivamente.
Todos los plástidos se desarrollan a partir de protoplástidos, que son organelos indiferenciados, carentes de membranas internas que se localizan en los meristemos de rápido crecimiento. Los protoplástidos se diferencian de acuerdo con el tejido en que se encuentran y las necesidades metabólicas de la célula. Es notable, por ejemplo, el cambio que sufren los cloroplastos hacia cromoplastos durante la maduración de los frutos: los cloroplastos pierden sus membranas tilacoides e inician la síntesis de nuevos tipos de carotenoides.
La formación de los cloroplastos a partir de los protoplástidos es un buen ejemplo de la interacción entre genoma y ambiente: la luz desencadena la formación de las enzimas necesarias para la fotosíntesis, los pigmentos que absorberán la luz se sintetizan rápidamente y se inicia la formación de las membranas tilacoidales y su estructuración en sacos tilacoides y grana.
Los fenómenos de transporte a través de la membrana, así como los procesos de endocitosis y exocitosis (estos últimos presentes sólo en eucariontes), son parte de los mecanismos que poseen las células para llevar a cabo un intercambio eficaz de materiales y energía con el exterior. Una vez en el interior celular, las sustancias serán transformadas a través de una serie de reacciones químicas, que en su conjunto reciben el nombre de metabolismo. La mayoría de las reacciones no ocurre de manera aislada, sino que se hallan organizadas en "cascadas" llamadas rutas o vías metabólicas, en las que el producto de una reacción es el sustrato para la siguiente y cada una es catalizada por una enzima específica.
La mayoría de los procesos metabólicos consiste en reacciones de óxido-reducción. En dichas reacciones, los electrones se mueven de niveles de energía mayores a menores, liberando energía que es utilizada por la célula en sus múltiples reacciones.
La pérdida de un electrón se denomina oxidación y la ganancia reducción. Estos procesos son simultáneos, pues para que ocurra la reducción debe existir una molécula que libere un electrón.
Los sistemas vivos, desde la célula hasta los organismos más complejos, realizan una gran variedad de actividades biosintéticas y todas ellas requieren de energía.
Una gran proporción de la energía (alrededor del 90%) es suministrada por el ATP, molécula que con su función asegura el conjunto de reacciones químicas que constituyen el metabolismo. La síntesis de proteínas, de ácidos nucléicos, las funciones de secreción y excreción celular y prácticamente todas las reacciones de la célula requieren de ATP.
El ATP es un nucleótido formado por un azúcar de cinco carbonos llamado ribosa, una adenina y tres grupos fosfato. La transferencia de un grupo fosfato se llama fosforilación. El ATP tiene varias cargas negativas muy próximas que tienden a desestabilizar a la molécula, así que cuando se hidroliza y cede un grupo fosfato adquiere mayor estabilidad transformándose en ADP, que en cualquier momento puede regenerarse y volver a su estado inicial de ATP. Las células hacen uso del ATP permanentemente; ya sea invirtiéndolo en reacciones que requieren energía o recuperándolo en reacciones que liberan energía.
El ATP es la sustancia más importante destinada a capturar y transferir energía en las células. La hidrólisis del fosfato terminal de esta molécula libera energía que sirve para impulsar las diversas actividades celulares, por ejemplo, la contracción de los músculos, el movimiento de moléculas en contra de un gradiente de concentración y la formación de péptidos.
La mayor parte del ATP que necesitan los sistemas biológicos proviene de la respiración celular y de la fotosíntesis. En el primer caso, en la mayoría de los organismos, la glucosa y los ácidos grasos son metabolizados hasta CO2 y H2O, y la energía liberada en las reacciones de oxidorreducción será aprovechada para efectuar el proceso de quimiosmosis, que se resume como el "bombeo" de protones hacia el espacio intermembranal de la mitocondria; la translocación de protones se efectúa a través de tres de los complejos pertenecientes a la cadena de transportadores de electrones localizados en la membrana interna de la mitocondria. Los protones acumulados en el espacio intermembranal regresarán a la matriz mitocondrial por medio de un complejo proteico denominado ATP sintetasa en el cual moléculas de ADP e iones fosfato se unen para formar las moléculas de ATP.
En la fotosíntesis, la energía procedente de las reacciones termonucleares del Sol es transformada en energía química de los enlaces de ATP, que posteriormente se almacenará en los compuestos orgánicos como almidón y sacarosa. Las plantas, las algas y algunos procariontes constituyen la base de la mayor parte de las cadenas alimentarias. La excepción está representada por las bacterias que habitan en las ventilas hidrotermales, las cuales utilizan reacciones de oxidación de compuestos inorgánicos reducidos, para obtener el ATP.
La fotosíntesis y la respiración, aparentemente distintos, tienen en común la quimiosmosis que indica que los procesos metabólicos han sufrido una evolución a partir de procesos comunes a través de miles de millones de años:
• La quimiosmosis en la fotosíntesis y en la respiración requiere de la presencia de una membrana impermeable a los protones y en la que se encuentre una cadena de transportadores de electrones. En ambos procesos, los hidrógenos procedentes del agua, en el caso de la fotosíntesis o de las moléculas orgánicas, en el caso de la respiración, se disocian en electrones y protones. Los electrones son llevados por una cadena de transportadores desde un nivel alto de energía a uno menor, y la energía liberada en los procesos de oxidorreducción permite que los protones sean "bombeados" de uno a otro lado de una membrana en contra de un gradiente electroquímico, a través de algunos complejos integrantes de la cadena de transportadores de electrones.
• A continuación, los protones acumulados en uno de los lados de la membrana (del cloroplasto, de la mitocondria o de la membrana plasmática en el caso de los procariontes) la atravesarán nuevamente, pero ahora lo harán a favor de un gradiente de concentración y a través de la ATP sintasa o sinteasa, en la que se efectuará la síntesis de la mayor parte del ATP que la célula utilizará para efectuar sus funciones.
La compleja organización que caracteriza a las células sólo puede mantenerse gracias al aporte constante de energía proveniente del exterior.
Con excepción de algunas especies de organismos unicelulares, la presencia de mitocondrias constituye un rasgo prácticamente universal de las células eucariontes, mientras los cloroplastos sólo se encuentran en algas y plantas fotosintetizadoras.
Catabolismo de la glucosa y de los ácidos grasos | Como se ha mencionado arriba, la célula ha desarrollado mecanismos para elaborar eficazmente ATP en la fotosíntesis y en la respiración. En la respiración, que se lleva a cabo en las mitocondrias de las células eucariontes, se utiliza el acetato de dos carbonos que deriva, por un lado, de la descomposición de la glucosa (denominada glucólisis) y, por otro, del catabolismo de los ácidos grasos (llamado beta oxidación).
La glucólisis es una vía metabólica muy interesante, desde el punto de vista evolutivo, debido a que se piensa que fue una de las maneras como las células primitivas obtenían energía. Se trata de una serie de reacciones que pueden dividirse en dos grandes grupos: las primeras son reacciones de activación energética en las cuales, la glucosa y su isómero fructosa, son fosforiladas por dos moléculas de ATP para formar una molécula de fructosa bifosfato.

En la segunda parte del proceso, la fructosa bifosfato se divide en dos moléculas de tres carbonos cada una: gliceraldehído 3 fosfato y dihidroxiacetona fosfato; esta última se transformará a su vez en gliceraldehído 3 fosfato.
A continuación, ambas moléculas de gliceraldehído sustituyen el hidrógeno del grupo funcional aldehído por un grupo fosfato; los hidrógenos son aceptados por la coenzima NAD que se transforma en NADH + H+. Por lo tanto, las dos moléculas de gliceraldehído, se transforman en dos moléculas 1,3 bifosfoglicerato. A continuación, éstas pierden los fosfatos de los carbonos 1, permitiendo que dos moléculas de ADP se transformen en dos moléculas de ATP. A esto se le denomina primera ganancia de energía. Siguen a continuación tres reacciones sucesivas que modifican la estructura de las moléculas, hasta llevarlas a un alto nivel energético, que permita la liberación de los fosfatos restantes para formar las dos últimas moléculas de ATP (segunda ganancia de energía).
Al final del proceso de glucólisis se forman dos moléculas de piruvato o ácido pirúvico y dos moléculas de NADH, cuyo destino dependerá de la presencia o no de oxígeno en el medio celular. De acuerdo con esto, los organismos pueden ser aerobios obligados, si para su existencia es necesario el oxígeno, pues éste es el aceptor final de electrones; en otros casos, ciertos organismos, como anélidos, moluscos o levaduras, que pueden desarrollarse en presencia o ausencia de oxígeno, se les llama anaerobios facultativos, ya que el aceptor de electrones puede ser el oxígeno o una sustancia orgánica.


La ausencia de oxígeno en el medio hace que el piruvato sea el aceptor final de electrones provenientes del NADH, que se formó en el paso de gliceraldehído a bifosfoglicerato; la sustancia que resulta es el ácido láctico y el proceso de su formación es la fermentación láctica. En la conocida fermentación alcohólica, que efectúa Saccharomyces cerevisiae, el aceptor final de electrones, es el acetaldehído que resulta de la descarboxilación del piruvato. Este proceso origina la mayor parte de las bebidas alcohólicas como vinos y cervezas, con formación de etanol, CO2 y NAD+.
En las células musculares de los mamíferos existe la fermentación láctica, que se presenta cuando el suministro de oxígeno es limitado; la glucosa presente en estas células inicia el proceso de glucólisis hasta piruvato pero, debido a la falta de oxígeno, no ingresa en la mitocondria, sino que actúa como aceptor de los electrones provenientes del NADH. El ácido láctico resultante es el responsable del dolor muscular. La mayor parte del lactato producido se secreta a la sangre y se recoge en el hígado, donde puede convertirse nuevamente en piruvato para seguir la vía aerobia o puede convertirse en glucosa por medio de la gluconeogénesis o formación de nueva glucosa.
La formación de glucosa a partir del lactato-piruvato va en sentido opuesto, siguiendo casi de manera idéntica los pasos de la glucólisis; este proceso que se presenta en las células animales, tiene una relación evolutiva interesante, como se verá más adelante en la primera parte del ciclo de Calvin de la fotosíntesis, en donde se sintetiza glucosa; en ella se utiliza una serie de reacciones similares a las que se efectúan en la gluconeogénesis de las células animales.
La presencia de oxígeno en el medio celular permite que el piruvato ingrese en la mitocondria, para seguir con la respiración celular, que se caracteriza porque el aceptor final de electrones es el oxígeno molecular, a diferencia de las fermentaciones, en las cuales el aceptor final de electrones es una sustancia orgánica (piruvato, acetaldehído, etcétera).
La respiración celular se subdivide en tres grupos de reacciones claramente distinguibles:
• Un preámbulo o puente al ciclo de Krebs, en el que el piruvato dentro de la matriz mitocondrial sufre una descarboxilación oxidativa, es decir, pierde bióxido de carbono e hidrógenos simultáneamente; al mismo tiempo, el acetato resultante se une a la coenzima A para dar acetilcoenzima A o acetilCoA. Los hidrógenos liberados enzimáticamente son recibidos por el NAD+ para dar NADH.
• La segunda serie de reacciones es el ciclo de Krebs (la vía metabólica por excelencia), que también se lleva a cabo en la matriz mitocondrial, se inicia con la unión o condensación del acetato de dos carbonos con el oxaloacetato de cuatro carbonos. La molécula resultante es el citrato de seis carbonos, la posterior formación de 3 NADH, 1 FADH2, 1 GTP, 2 CO2 y renovación de la molécula de cuatro carbonos.
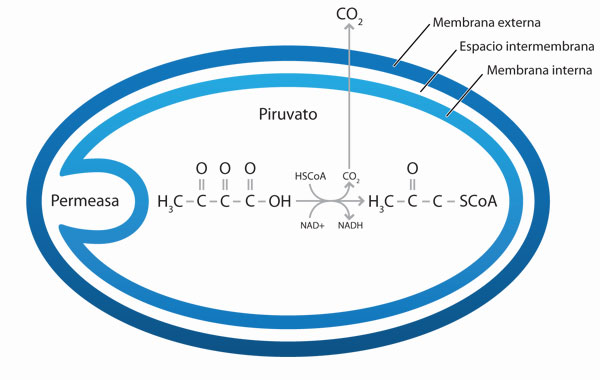
La siguiente serie de reacciones enzimáticas elimina dos moléculas de bióxido de carbono e hidrógenos que son aceptados por las coenzimas NAD+ y FAD+; además, a la mitad del ciclo se forma una única molécula de ATP. La pérdida de carbonos ocasiona que las moléculas de seis carbonos, paulatinamente se transformen, primero en una molécula de cinco carbonos y finalmente en moléculas de cuatro carbonos, siendo la última de la serie el oxaloacetato, con la cual se inicia nuevamente el ciclo. La importancia del ciclo de Krebs radica en la formación de NAD+ y FAD+ reducidos (NADH H+ y FADH2).
¿Por qué el acetato tiene que ingresar en el ciclo de Krebs, en lugar de oxidarse directamente? La respuesta radica en que el metilo de esta sustancia no puede ser oxidado fácilmente para dar bióxido de carbono; por esta razón tiene que unirse al oxaloacetato, para oxidarse de manera indirecta; algo similar ocurre en el inicio del ciclo de Calvin, cuando el bióxido de carbono se une a la ribulosa bifosfato para reducirse indirectamente y poder "transformarse" en glucosa.
• La tercera serie de reacciones de la respiración se realiza en la membrana interna de la mitocondria, o en el caso de los procariontes, en la membrana plasmática. Los hidrógenos que provienen del ciclo de Krebs y que son llevados por el NAD+ y FAD+ se disocian en electrones y protones. Los electrones son transportados a través de una serie de complejos proteicos denominada cadena transportadora de electrones o cadena respiratoria; la energía liberada durante el paso de los electrones permite que los protones sean "bombeados" en contra de un gradiente de concentración, de la matriz hacia el espacio intermembranal, en los complejos I, II y IV.
El movimiento de protones de regreso a la matriz y a favor de un gradiente de concentración, se hace a través de la ATP sintasa, que aprovecha la corriente de protones para acoplar el ADP con un fosfato y formar ATP; el proceso, como ya se mencionó, es la quimiosmosis o fuerza motriz de protones. Finalmente, tanto electrones como protones son aceptados por el oxígeno para formar agua.

Para calcular la cantidad de moles de ATP que se producen en la oxidación completa de un mol de glucosa debemos considerar los aspectos siguientes:
a] En la glucólisis se producen directamente dos moles de ATP.
b] En el mismo proceso se obtienen dos moles de NADH, mismos que mandan sus hidrógenos a la mitocondria, no directamente, sino a través de dos sustancias distintas, que depositan los hidrógenos en el NAD+ o FAD+ de este organelo.
c] En el preámbulo al ciclo de Krebs, los dos moles de piruvato que se transforman en dos de acetato, forman dos moles de NADH.
d] En el ciclo de Krebs, la oxidación de cada mol de acetato producirá tres moles de NADH, un mol de FADH2 y un mol de ATP.
e] Por cada mol de NADH2 que ingresa a la cadena respiratoria se forman tres moles de ATP y por cada mol de FADH se obtienen dos moles de ATP.
f] Para calcular correctamente la cantidad de ATP que se forma en el proceso de oxidación de la glucosa, es necesario tener presente que la glucosa forma dos moléculas de piruvato y que cada una de ellas se transformará en acetato y se oxidará completamente en el ciclo de Krebs.
Por lo tanto, ¿cuántos moles de ATP se obtienen por cada mol de glucosa?

Así como la glucosa sigue la ruta de la glucólisis antes de entrar en el proceso de respiración, los ácidos grasos almacenados en forma de triacilglicéridos primero se hidrolizan separándose del glicerol. Al ser depositados en la sangre, los ácidos grasos son llevados a la mayoría de las células para ser oxidados, principalmente en la mitocondria. El proceso de oxidación de estas sustancias se denomina b-oxidación; en ella se forman moléculas de acetilCoA y NAD+ y FAD+ reducidos. Las moléculas de acetato ingresan en el ciclo de Krebs, mientras las coenzimas NAD+ y FAD+ reducidas directamente van a la cadena respiratoria.
La cantidad de ATP que se forma de la completa oxidación de un ácido graso depende del tamaño de éste; por ejemplo, en la oxidación completa de un mol de ácido graso de 18 carbonos se obtienen nueve moles de acetato, ocho moles de NADH y ocho moles de FADH2.
El cálculo se hace de la siguiente manera: de cada mol de acetato se obtienen tres moles de NADH, un mol de FADH y un mol de ATP. Por lo tanto, de cada acetato se obtienen 12 moles de ATP.

En total: 143 moles de ATP menos un mol de ATP que se usó para activar energéticamente al ácido graso al inicio de la b-oxidación. De lo anterior se desprende la importancia de los ácidos grasos como sustancias altamente energéticas, pues se obtiene una cantidad considerablemente mayor de energía si se compara con la obtenida por cada mol de glucosa oxidado completamente.
Fotosíntesis| De acuerdo con lo mencionado antes, la célula es un sistema abierto que necesita un aporte continuo de energía. Ésta se encuentra siempre disponible, pues proviene de los procesos de fusión nuclear que se efectúan en el Sol. Los átomos de hidrógeno que se encuentran en esa estrella, continuamente se fusionan para formar átomos de helio, electrones libres y fotones.
Parte de la energía se desprende como radiaciones gamma y es absorbida por los electrones producidos en el Sol; mientras la mayor parte es emitida en longitudes de onda mayor, pudiendo ser absorbida y transmitida como energía química, gracias a la presencia de las porfirinas que forman parte fundamental de las clorofilas, que se encuentran en las membranas de los procariontes fotosintetizadores y en los cloroplastos de las algas y plantas terrestres.
El proceso de transformación de la energía radiante en energía química es la fotosíntesis, cuyos productos finales son la glucosa, la sacarosa y el almidón. En este proceso se obtiene también oxígeno como subproducto, el cual es el eslabón que comunica con la respiración, cerrándose de esta manera el principal ciclo de la vida.
La reacción general de la fotosíntesis oxigénica (que produce oxígeno)
6CO2 + 6H2O → 6O2 + C6H12O2 corresponde a la reacción inversa del proceso general, en la cual los carbohidratos son oxidados completamente a CO2 y H2O. Ciertos procariontes como las bacterias verdes y las púrpuras también fotosintetizan, pero no producen oxígeno.

La fotosíntesis es un proceso muy complejo que se subdivide en cuatro fases, tres de las cuales requieren de la luz para realizarse:
• Absorción de la energía radiante.
• Rompimiento del agua, liberación del oxígeno, transporte de electrones a través de una cadena de sustancias, reducción del NADP+ a NADPH y acumulación de protones en el interior del tilacoide.
• Síntesis de ATP.
• Conversión del CO2 en carbohidratos o fijación del carbono.
Las enzimas necesarias para las tres primeras etapas se localizan en las membranas tilacoidales; las que se necesitan para la fijación del carbono y su transformación posterior en almidón se localizan en el estroma del cloroplasto; mientras las enzimas que forman sacarosa se encuentran en el citosol.
Absorción de energía radiante, transporte de electrones y síntesis de ATP | Éste es el paso inicial del proceso fotosintético; para que se lleve a cabo es necesaria la presencia de las clorofilas que son pigmentos asociados con proteínas localizadas en las membranas tilacoidales. Constan de un núcleo de porfirina unido a una larga cadena hidrocarbonada denominada fitol. El núcleo de porfirina es similar al hem de la hemoglobina, pero a diferencia de éste, en lugar de un ion de Fe2+ tiene un ion de Mg2+ y un anillo adicional.
La energía absorbida por el anillo de porfirina se usa para quitarle electrones, lo cual provoca que la clorofila se vuelva un eficaz agente reductor.

Los "huecos" de electrones dejados en la clorofila son llenados con los electrones del agua; ésta se rompe gracias a la presencia de un complejo enzimático que posee manganeso. El oxígeno se libera rápidamente, mientras los hidrógenos se disocian en electrones y protones. Al igual que en la respiración, los electrones son llevados a través de una cadena de transportadores, hasta que llegan a su último aceptor que es el NADP+, el cual se transforma en NADPH, que es casi idéntico al NAD+, sólo que tiene un fosfato adicional.
Los protones que resultan de la disociación de los hidrógenos se acumulan en el lumen o luz tilacoidal y pasan a favor de un gradiente electroquímico por la ATP sintasa para formar el ATP; la síntesis de ATP es idéntica a la que se realiza en la mitocondria, lo cual evidencia su relación evolutiva.
Un análisis más detallado de las reacciones dependientes de la luz, muestra que los organismos fotosintetizadores que producen oxígeno forman grandes complejos denominados fotosistemas I y II, constituidos por proteínas asociadas a una clorofila especial (denominada centro de reacción) y clorofilas y carotenoides que actúan como antenas recolectoras de diferentes longitudes de onda. Las bacterias fotosintetizadoras que no producen oxígeno sólo presentan el fotosistema I.
Ambos fotosistemas se encuentran, junto con los transportadores de electrones, en las membranas tilacoidales del cloroplasto, pero difieren en sus funciones: el fotosistema II, es el único que tiene capacidad para romper el agua, mientras el fotosistema I es el que forma el poder reductor o NADPH.
El centro de reacción del fotosistema II (P680), constituido por dos moléculas especiales de clorofila a, recibe la energía capturada por los pigmentos antena, y la utiliza para mandar uno de sus electrones a un nivel superior de energía; el electrón no regresa a su nivel original sino que reduce rápidamente al primer integrante de la cadena transportadora de electrones. Las reacciones de oxidorreducción que se efectúan al paso de los electrones liberan energía para el traslado de protones desde el estroma hasta el lumen tilacoidal, mismos que aunados a los provenientes del agua, garantizan un aporte suficiente de protones para que se sintetice ATP.
Los electrones, después de haber pasado por diferentes transportadores, llegan al fotosistema I, cuyo centro de reacción (P700) al ser estimulado por un fotón, libera nuevamente un electrón que finalmente, después de ser transportado por diferentes sustancias, reducirá el NADP a NADPH.
La síntesis de ATP y de NADPH es imprescindible para que se efectúe la siguiente etapa de la fotosíntesis: el ciclo de Calvin, serie de reacciones de biosíntesis por medio de las cuales la mayoría de los organismos fotosintetizadores convierte el CO2 en compuestos orgánicos.
Conversión de CO2 en carbohidratos | Los cloroplastos de las plantas y de las algas son sitios de intensa actividad metabólica; en ellos se producen casi todos los aminoácidos, los ácidos grasos y los carotenos, las pirimidinas y posiblemente todas las purinas; sin embargo, la más importante aportación de los cloroplastos es la fijación del CO2 que derivará en la síntesis de carbohidratos.
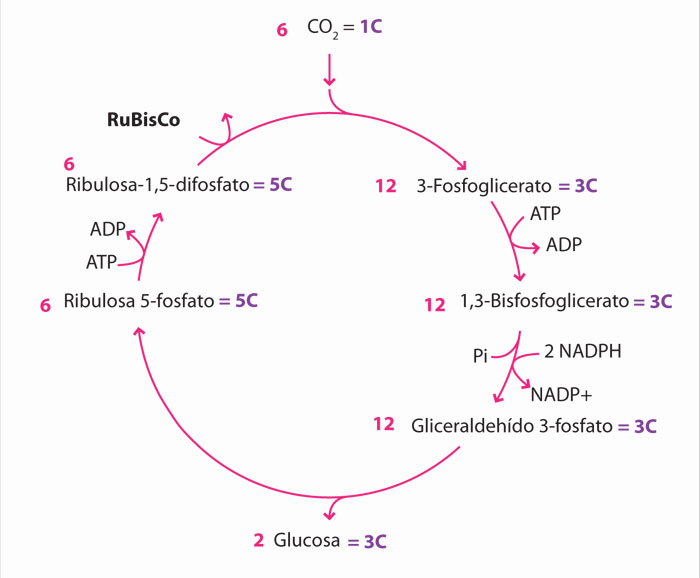
El ciclo de Calvin (en honor a su descubridor Melvin Calvin) se inicia con la fijación de CO2 a una molécula de ribulosa bifosfato; esta reacción es catalizada por la enzima ribulosa 1, 5- bifosfato carboxilasa conocida comúnmente como RuBisCo, que se localiza en el estroma de los cloroplastos. Inmediatamente después se forma un intermediario de seis carbonos que pronto se divide para formar 3-fosfoglicerato o ácido fosfoglicérico. El cual es fosforilado por ATP para formar moléculas de 1, 3-bifosfoglicerato, mismas que serán reducidas por el NADP+ para formar gliceraldehído 3 fosfato; estas reacciones forman parte de un proceso de gluconeogénesis, que culminará con la formación de glucosa.
El ciclo de Calvin se cierra con una segunda serie de reacciones que lleva al reciclaje de la ribulosa 1, 5-bifosfato, sin el cual no habría fijación de CO2.

Fotorrespiración | La enzima rubisco, no sólo permite la fijación del CO2: en condiciones de baja concentración de CO2 y alta de O2 favorece la adición de O2 al 3-fosfoglicerato en el cloroplasto para formar una molécula de fosfoglicolato, que pasa a los peroxisomas donde se transforma en glicina que, al pasar a la mitocondria, pierde CO2; la sustancia resultante tiene una serie de reacciones conforme pasa nuevamente a peroxisoma, hasta llegar al cloroplasto, en donde se incorpora al ciclo de Calvin en forma de 3-fosfoglicerato.
• La fotorrespiración actúa en contra del proceso de fotosíntesis, puesto que:
– No permite que la ribulosa 1, 3-bifosfato fije el CO2.
– Consume O2 y libera CO2.
– Utiliza ATP innecesariamente.
A pesar de que actualmente no representa una vía útil para las plantas, se especula que la fotorrespiración tuvo una importancia evolutiva en las etapas en las que el O2 era altamente tóxico para los organismos, siendo este proceso indispensable para regular la cantidad de O2 que podían tolerar los organismos primitivos.
En vista de que la fotorrespiración disminuye la capacidad fotosintetizadora, actualmente se pretende modificar genéticamente las plantas de valor económico con el fin de aumentar su rendimiento.
La fotorrespiración se reduce en las plantas que fijan el CO2 por medio de la vía C4. Son plantas que habitan en un medio muy seco, y que por lo tanto necesitan cuidarse del exceso de evaporación cerrando sus estomas. Esto hace que la concentración interna de CO2 sea bastante baja, por lo que se favorece la fotorrespiración; sin embargo, las plantas como el maíz y la caña de azúcar evitan este problema al utilizar la vía C4, llamada así porque al aceptarse el CO2 se forma una sustancia de cuatro carbonos, como el oxaloacetato, en lugar del 3 fosfoglicerato de tres carbonos que se forma en el ciclo de Calvin.
La vía C4 requiere de dos tipos de células: las células de la vaina, que rodean el haz vascular, y las células del mesófilo, que se encuentran rodeando a las anteriores. En las células del mesófilo que se encuentran en contacto con el CO2 que entra por los estomas, una molécula de tres carbonos recibe este gas para generar una molécula de cuatro carbonos; las moléculas de cuatro carbonos se introducen en las células de la vaina, en donde liberan el CO2, el cual se incorpora al ciclo de Calvin. La molécula de tres carbonos que queda regresa a las células del mesófilo para recibir otra molécula de CO2. La enzima que cataliza esta reacción se encuentra exclusivamente en las plantas C4. Gracias a este proceso, a pesar de que las células fotosintetizadoras se encuentran en un medio de baja concentración de CO2, pueden efectuar la fijación de éste con eficacia.